
Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Хиперпластични процеси ендометријума
Медицински стручњак за чланак
Последње прегледано: 04.07.2025
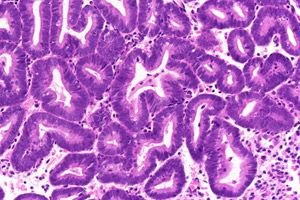
Епидемиологија
Хиперпластични процеси ендометријума су могући у било ком узрасту, али њихова учесталост значајно расте до периода перименопаузе. Према већини научника, хиперпластични процеси ендометријума сматрају се прекурсорима самог рака ендометријума. Једноставна ендометријална хиперплазија без атипије развија се у рак у 1% случајева, полипоидни облик без атипије - 3 пута чешће. Једноставна атипична ендометријална хиперплазија без лечења прогресира у рак код 8% пацијената, сложена атипична хиперплазија - код 29% пацијената.
Најчешћи тип хиперпластичног процеса ендометријума су полипи, који се јављају код гинеколошких пацијенткиња са учесталошћу до 25%. Ендометријски полипи се најчешће откривају у пре- и постменопаузи. Ендометријски полипи постају малигни у 2–3% случајева.
Узроци хиперпластични процеси ендометријума
Најчешће се хиперпластични процеси ендометријума дијагностикују код жена са повећаним концентрацијама естрогена било које генезе. Повишени нивои естрогена код жена које узимају хормонску терапију замене (ХРТ) повећавају ризик од развоја ендометријалне хиперплазије. Тамоксифен се сматра ефикасним у лечењу пацијената са раком дојке, али његова употреба повећава ризик од развоја хиперпластичних процеса ендометријума.
Симптоми хиперпластични процеси ендометријума
Главне клиничке манифестације хиперпластичних процеса ендометријума су крварење из материце, често ациклично у облику метрорагије, ређе менорагије. Понекад су полипи ендометријума асимптоматски, посебно у постменопаузи.
Пошто је патогенетска основа ендометријалних хиперпластичних процеса ановулација, водећи симптом код пацијенткиња репродуктивног доба је неплодност, обично примарна.
Шта те мучи?
Обрасци
Постоје три главна типа хиперпластичних процеса ендометријума: ендометријална хиперплазија, ендометријални полипи и атипична хиперплазија (аденоматоза).
Године 1994, СЗО је усвојила класификацију ендометријалне хиперплазије на основу препорука водећих гинеколога и патолога, укључујући хиперплазију без ћелијске атипије и хиперплазију са ћелијском атипијом (атипична ендометријална хиперплазија или аденоматоза). У свакој групи се разликују једноставна и сложена хиперплазија, у зависности од тежине пролиферативних процеса у ендометријуму.
Ендометријски полип је бенигна туморолика формација која потиче из базалног слоја ендометријума. Патогномонична анатомска карактеристика ендометријалног полипа је његова база, „педикул“. У зависности од хистолошке структуре, постоје жлездани (функционални или базални тип), жлездано-фиброзни, фиброзни и аденоматозни полипи ендометријума. Аденоматозни полипи карактеришу се интензивном пролиферацијом жлезда и њиховог епитела са релативно високом митотском активношћу. Аденоматозни полипи се сматрају преканцерозним стањима. Жлездани полипи су најтипичнији за репродуктивни период, жлездано-фиброзни - за пре- и перименопаузу, фиброзно-жлездани и фиброзни - за постменопаузу.
У репродуктивном и пременопаузалном периоду живота жене, ендометријални полипи као хистолошки независан облик могу се одредити и на позадини ендометријалне хиперплазије и са нормалном слузокожом различитих фаза менструалног циклуса.
Ендометријски полипи у постменопаузи су обично појединачни и могу се јавити на позадини атрофичне слузокоже. У постменопаузалном периоду, ендометријални полипи понекад достижу велике величине и протежу се изван грлића материце, чиме имитирају цервикални полип.
Концепт „рецидива“ ендометријалног полипа је неприхватљив ако претходно није коришћена хистероскопска контрола током уклањања ендометријалног полипа, јер стругање слузокоже материце без хистероскопије може оставити патолошки измењено ткиво.
Са морфолошког становишта, ендометријални преканцер обухвата хиперплазију са атипијом (атипичну хиперплазију) и аденоматозне полипе.
Дијагностика хиперпластични процеси ендометријума
Поред општеприхваћених метода испитивања, важна тачка је идентификација пратећих болести и процена стања јетре, кардиоваскуларног система (КВС), гастроинтестиналног тракта (ГИТ), јер је то важно при избору методе лечења, посебно при именовању хормонске терапије.
Главне методе дијагностиковања хиперпластичних процеса ендометријума у садашњој фази укључују цитолошки преглед аспирата из материчне дупље, трансвагинални ултразвук, хидросонографију и хистероскопију. Међутим, дијагноза се може коначно потврдити тек након хистолошког прегледа ендометријума, добијеног одвојеном дијагностичком киретажом слузокоже материце.
Цитолошки преглед аспирата из материчне шупљине препоручује се као скрининг тест за патологију ендометријума и одређивање његовог стања у динамици на позадини хормонске терапије. Ова метода омогућава одређивање тежине пролиферативних промена, али не даје јасну представу о његовој патоморфолошкој структури.
Трансвагинално ултразвучно скенирање је вредна метода за дијагностиковање хиперпластичних процеса ендометријума због високог садржаја информација, неинвазивности и безбедности за пацијента. Ултразвук омогућава процену не само стања ендометријума, већ и миометријума, као и идентификацију аденомиозе и миома материце. Ултразвук треба урадити и ради одређивања величине јајника и процене њихових функција.
Дијагноза ендометријалне хиперплазије ултразвуком заснива се на откривању увећане антеропостериорне величине средњег утериног еха (М-еха) са повећаном акустичном густином. Код жена које менструирају, дебљину М-еха треба проценити у складу са фазом менструалног циклуса. Најбоље је спровести студију одмах након менструације, када танак М-ехо одговара потпуном одбацивању функционалног слоја ендометријума, а повећање антеропостериорне величине М-еха дуж целе његове дужине, или локално, сматра се патологијом. Немогуће је разликовати жлездану хиперплазију ендометријума од атипичне ултразвуком.
Ако постменопаузални период не прелази 5 година, дебљина М-еха до 5 мм се сматра нормалном, са постменопаузом више од 5 година, дебљина М-еха не би требало да прелази 4 мм (са хомогеном структуром). Тачност ултразвучне дијагностике за хиперпластичне процесе ендометријума је 60-70%.
Хидросонографија може значајно побољшати дијагностичке резултате. Ултразвучна слика ендометријалних полипа показује јајолике, ређе округле инклузије у структури М-еха и материчне шупљине са повећаном густином еха. Дијагностичке потешкоће настају код жлезданих полипа ендометријума, који имају листолику или спљоштену конфигурацију у облику материчне шупљине и нису способни да доведу до задебљања М-еха. У погледу проводљивости звука, они су близу околног ендометријума. Регистрација колор ехо сигнала током Доплеровог прегледа у структури инклузије омогућава разликовање полипа од интраутериних адхезија, а код менструирајућих пацијенткиња - од крвних угрушака, али проток крви у полипима није увек одређен током колор дуплекс мапирања. Информативни садржај трансвагиналног ултразвука за ендометријалне полипе је 80-90%. Контрастирање материчне шупљине током хидросонографије може повећати дијагностичке могућности ултразвука. Трансвагинална хидросонографија и биопсија ендометријума омогућавају дијагностиковање ГПЕ у 98%.
Информативна вредност хистероскопије у дијагностици хиперпластичних процеса ендометријума је 63–97% (у зависности од врсте хиперпластичних процеса ендометријума). Хистероскопија је неопходна и пре киретаже слузокоже материце ради разјашњења природе патологије и њене локализације, и након ње ради контроле темељности уклањања ткива. Хистероскопија омогућава визуелну процену стања зидова материце, идентификовање аденомиозе, субмукозног миома материце и других облика патологије. Атипична ендометријална хиперплазија нема карактеристичне ендоскопске критеријуме, хистероскопска слика подсећа на обичну жлездану цистичну хиперплазију. Код тешке атипичне хиперплазије могу се идентификовати жлездани полипоидни израштаји тамно жућкасте или сивкасте боје.
Хистолошки преглед стругања слузокоже материце је дефинитивна метода за дијагностиковање хиперпластичних процеса ендометријума.
 [ 26 ]
[ 26 ]
Шта треба испитати?
Кога треба контактирати?
Третман хиперпластични процеси ендометријума
Терапија за жене различите старости састоји се у заустављању крварења, обнављању менструалне функције током репродуктивног периода или постизању менопаузе у старијој доби, као и спречавању поновног појављивања хиперпластичног процеса.
Лечење хиперпластичних процеса ендометријума код пацијената репродуктивног доба
Хормонска терапија се сматра традиционалном методом лечења хиперпластичних процеса ендометријума.
Рецидиви ендометријалног хиперпластичног процеса указују на недовољну терапију или хормонски активне процесе у јајницима, што захтева разјашњење њиховог стања, укључујући визуелне дијагностичке методе (ултразвук, лапароскопија, биопсија јајника). Одсуство морфолошких промена у јајницима омогућава наставак хормонске терапије вишим дозама лекова. Потребно је искључити инфективни фактор као могући узрок болести и неефикасност хормонске терапије.
Ако је хормонска терапија неефикасна или дође до рецидива ендометријалне хиперплазије без атипије, препоручљива је аблација (ресекција) ендометријума. Аблација ендометријума може се извести различитим методама: коришћењем моно- и биполарних коагулатора, ласера и балона. Неопходни услови за извођење аблације: жена не жели да има децу у будућности, старија је од 35 година, жели да сачува материцу и величина материце није већа од 10 недеља трудноће. Матерични фиброми се не сматрају контраиндикацијом за ендометријалну аблацију; ако ниједан од чворова не прелази 4–5 цм, онда аденомиоза погоршава резултате операције.
Поновна појава атипичне ендометријалне хиперплазије код пацијената репродуктивног доба је индикација за детаљно испитивање и искључивање синдрома полицистичних јајника.
Лечење у пре- и перименопаузи
Прва фаза лечења обухвата хистероскопију са одвојеном дијагностичком киретажом слузокоже материце. Избор даље терапије зависи од морфолошке структуре ендометријума, истовремене гинеколошке и екстрагениталне патологије. Избор хормонског лека, шема и трајање лечења такође су одређени потребом за одржавањем ритмичне менструалне реакције (до 50. године) или упорним престанком менструације.
У случају рекурентне ендометријалне хиперплазије без атипије, немогућности хормонске терапије због истовремене екстрагениталне патологије, индикована је хистероскопска хирургија - аблација ендометријума. Рецидиви ендометријалних хиперпластичних процеса, као и комбинација ове патологије са миомом материце и/или аденомиозом код пацијенткиња у пре- и перименопаузи су индикације за хируршку интервенцију (хистеректомију).
Лечење у постменопаузи
Одвојена дијагностичка киретажа са хистероскопијом је индикована код пацијената са сумњом на ендометријалну патологију откривену током скрининг прегледа. У случају новооткривене ендометријалне хиперплазије код жена у постменопаузи, препоручљиво је прописати хормонску терапију.
У случају атипичне ендометријалне хиперплазије у постменопаузи, неопходно је одмах одлучити о радикалној операцији - панхистеректомији. У случају тешке екстрагениталне патологије и повећаног ризика од хируршког лечења, дозвољено је дуготрајно лечење хормонским лековима назначеним у Табели 3.
На позадини хормонске терапије, препоручљиво је препоручити хепатопротекторе, антикоагуланте и антитромбоцитна средства у нормалним дозама.
Поновна појава ендометријалне хиперплазије у постменопаузи је индикација за хируршку интервенцију: хистероскопску аблацију ендометријума или екстирпацију материце са додацима. Суправагинална ампутација материце са додацима је прихватљива (у одсуству патологије грлића материце).
Главна метода лечења пацијената са ендометријалним полипима у постменопаузи је циљана полипектомија. Радикално уклањање ендометријалног полипа (са базалним слојем на месту локализације полипа) могуће је само уз употребу хистероскопске опреме. За полипектомију се могу користити и механички ендоскопски инструменти и електрохируршка технологија, као и ласер. Електрохируршка ексцизија полипа током хистероскопије се препоручује код фиброзних и паријеталних полипа ендометријума, као и код рекурентних ендометријалних полипа.
Након уклањања жлезданих и жлездано-фиброзних полипа ендометријума, препоручљиво је прописати хормонску терапију. Врста хормонске терапије и њено трајање зависе од морфолошке структуре полипа и пратеће патологије.
Хормонска терапија за ендометријалне полипе у постменопаузи
| Припрема | Жлездани влакнасти, влакнасти полипи | Жлездани полипи |
| Норетистерон | 5 мг/дан током 6 месеци | 10 мг/дан током 6 месеци |
| Хидроксипрогестерон капроат | 250 мг једном недељно током 6 месеци | 250 мг 2 пута недељно током 6 месеци |
| Медроксипрогестерон | 10–20 мг/дан током 6 месеци | 20–30 мг/дан током 6 месеци |
Даље управљање
Пацијенткиње са ендометријалном хиперплазијом треба да буду под диспанзерским надзором најмање 2 године након престанка хормонске терапије; у случају атипичне хиперплазије (ако је спроведена хормонска терапија), период диспанзерског надзора треба да буде најмање 5 година. Ултразвук карличних органа и цитолошки преглед аспирата сваких 6 месеци су обавезни. Осетљивост ендометријалне биопсије помоћу Пипела је 99% за одређивање рака ендометријума и 75% за ендометријалну хиперплазију код жена у постменопаузи. Ако се патологија открије ултразвуком и цитолошким прегледом, индикована је хистероскопија и одвојена дијагностичка киретажа слузокоже материце са хистолошким прегледом стругања. Рецидив ендометријалних хиперпластичних процеса служи као основа за ревизију тактике лечења. Ако је пацијенткиња примила хормонску терапију у потпуности, треба поставити питање аблације (у одсуству патологије у јајницима) или хистеректомије.
Тешкоће у лечењу пацијената представљају пацијенткиње које су подвргнуте аблацији или ресекцији ендометријума, након чега се могу јавити синехије у материчној дупљи. Ултразвучни преглед ових пацијенткиња треба да обави специјалиста који је вешт у тумачењу ехографских знакова синехија. Међутим, присуство крвавог исцедка код ових пацијенткиња служи као индикација за хистероскопију и одвојену дијагностичку киретажу слузокоже материце у специјализованој гинеколошкој установи.

