
Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
„Кисеоник за ћелије“: једноставан имплант је помогао у снижавању нивоа шећера без јаких лекова
Последње прегледано: 18.08.2025
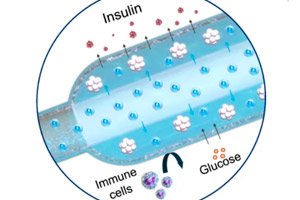 ">
">Нови „кисеонични“ имплантат за лечење дијабетеса типа 1 описан је у часопису Nature Communications: компактни електрохемијски генератор кисеоника (iEOG) континуирано снабдева O₂ макрокапсулу са ћелијама које луче инсулин. Овај систем омогућава чврсто паковање изолованих острваца (до 60.000 IEQ/ml) и одржава њихову одрживост и секрецију чак и у условима ниског садржаја кисеоника. Код пацова са дијабетесом, уређај имплантиран под кожу одржавао је нормалан ниво шећера до три месеца — без имуносупресије. Контролни пацови, без кисеоника, остали су хипергликемични.
Позадина
- Главни технички проблем је кисеоник. Чим „сакријемо“ ћелије иза мембране и ставимо уређај испод коже (згодно и лако се извлачи), оне немају кисеоник: дифузија кроз мембрану и слабо васкуларно место не задовољава потребе „прождрљивих“ острваца. Отуда рана смрт, слаб рад и потреба за знатним проређивањем сетве – у супротном капсула испада огромна.
- Зашто је то физички тако тешко? Кисеоник пролази кроз ткива само на веома кратким растојањима, а инкапсулиране ћелије немају сопствене крвне судове - првих месеци живе само захваљујући пасивној дифузији. Било какво згушњавање материјала или „збијање“ ћелија брзо преноси центар капсуле у хипоксију.
- Шта си раније пробао/пробала?
- Направили су макроуређаје који се могу поново пунити кисеоником (на пример, βAir): унутра се налази резервоар који се свакодневно допуњава кисеоником; спроведена су претклиничка и рана клиничка испитивања. Ради, али захтева много рада за пацијента.
- Испробани су хемијски донори O₂ и „носећи“ материјали (перфлуоро једињења): помажу, али дају краткотрајан и тешко контролисан ефекат. Појавили су се и „ваздушни“ оквири за убрзавање испоруке O₂ у дебљину гела.
- Саме капсуле и места имплантације (танке мембране, преваскуларизација) су побољшани, али без спољашњег извора О₂ и даље се суочавају са границама густине ћелија.
- Коју празнину у слагалици попуњава нови рад? Аутори часописа „Nature Communications“ приказују континуирано снабдевање кисеоником из мини-генератора директно унутар система макроенкапсулације: уређај узима воду из ткива и електрохемијски ослобађа O₂, који равномерно „дише“ дуж капсуле са ћелијама. Идеја је да се капсули да „сопствени акваријумски компресор“ како би могла да спакује више ћелија, а да их и даље одржава живима и раде – чак и на поткожном, не баш „оксигенисаном“ месту.
Зашто је ово уопште потребно?
Трансплантација острваца или бета ћелија један је од најперспективнијих путева ка „функционалном леку“ за дијабетес типа 1. Али постоје две главне препреке:
- Имунитет - обично захтева доживотне имуносупресоре;
- Кисеонично гладовање - капсуле које штите имуни систем истовремено одвајају ћелије од крвних судова, а бета ћелије, прождрљиве за О₂, брзо се „гуше“. Нови рад наилази на другу баријеру: даје капсули сопствени, контролисани извор кисеоника.
Како имплант функционише
- Два дела. У титанијумском кућишту налази се мини-генератор кисеоника (iEOG), који извлачи воду из интерстицијалне течности и ослобађа O₂ електролизом; поред њега се налази танка линеарна капсула са ћелијама (слична дугачкој „кобасици“), кроз коју пролази гасопропусна цев: кисеоник се равномерно апсорбује дуж целе капсуле. Између ћелија и ткива налази се полупропусна мембрана (електроспин + алгинат): глукоза и инсулин пролазе, имуне ћелије не.
- Димензије: Друга верзија iEOG-а је пречника 13 мм и дебљине 3,1 мм, тежине око 2 г. Када се упари са капсулом, такав систем се може убацити и уклонити кроз мали рез, што је важно за безбедност.
- Продуктивност. Генератор производи ~1,9–2,3 цм³ O₂/х и одржава задати проток месецима, па чак и годинама (у дугорочним тестовима у физиолошком раствору — до 2,5 године), а након имплантације код пацова, овај ниво је одржаван. Такав проток је израчунат да покрије потребе стотина хиљада еквивалената острваца — реда величине који је потребан особи.
Шта су експерименти показали
- Ин витро: При 1% О₂ (тешка хипоксија), оксигенација је одржавала одрживост и секрецију у агрегатима INS-1 и у људским острвцима упакованим у веома густ слој (60.000 IEQ/mL).
- Ин виво (пацови). Након поткожне имплантације у алогеном моделу дијабетеса, iEOG систем је нормализовао гликемију до 3 месеца без имуносупресије; уређаји без кисеоника нису имали ефекта. Хистологија око генератора није показала значајне нежељене реакције.
Зашто је ово важно за клинику?
- Корак ка „реалним димензијама“. Да би се одраслој особи обезбедила доза од 300–770 хиљада IEQ, капсула мора бити чврсто упакована – то је увек било ограничено кисеоником. Контролисано снабдевање O₂ „уклања плафон“ густине и даје шансу да се уређај учини довољно компактним за стварну имплантацију.
- Плус погодност. Раније смо пробали хемијске доноре кисеоника (пероксиде) - они не делују дуго и не могу се контролисати, као и резервоаре О₂ са свакодневним „допуњавањем“ кроз кожу - гломазно и незгодно. Овде се кисеоник доводи стално и у одмереним дозама, без ињекција.
Технички детаљи који импресионирају
- Извор воде је ткиво. iEOG усисава пару интерстицијалне течности кроз порозни „прозор“, а затим се класични мембранско-електродни склоп (MEA) и напон од 1,4–1,8 V користе за раздвајање воде на H₂ и O₂; гасови се уклањају кроз различите канале.
- Трајност. Три уређаја у физиолошком раствору радила су 11 месеци, 2 године и 2,5 године на једносмерној струји без деградације протоком кисеоника; након имплантације код имунодефицијентних и имунокомпетентних пацова, перформансе су одржане.
Ограничења и „шта даље“
Ово је још увек преклиничко: пацови, висока густина у капсули, снабдевање кисеоником - све је одлично, али кључни тестови су пред нама:
- прилагођавање дозама и временским оквирима за људе;
- поузданост и напајање електрохемичара у људском телу годинама (архитектура напајања није детаљно описана у чланку);
- минимизирање фиброзе око капсула и стабилност дифузије;
- тестирање на бета матичним ћелијама и на моделима ближим људима. Аутори отворено упоређују своје решење са претходним приступима и позиционирају га као платформу за клинички транслабилне капсуле.
Закључак
Да би трансплантиране бета ћелије живеле и функционисале без имуносупресора, потребно им је да дишу. Тим са Корнела и партнера показао је да мини-генератор кисеоника уграђен у линеарну капсулу може да „храни“ ћелије са O₂ довољно дуго и равномерно да издрже високу густину и смање шећер чак и на поткожној локацији. Клиника је још увек далеко, али инжењерска логика је једноставна и лепа - дати ћелијама ваздух тамо где га недостаје.
