
Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Неуролептици или антипсихотици
Медицински стручњак за чланак
Последње прегледано: 04.07.2025
Антипсихотици (неуролептици) су класа психотропних лекова који се првенствено користе за лечење шизофреније. Тренутно је уобичајено разликовати две групе (или категорије) лекова: типичне и атипичне антипсихотике. У наставку су дате информације о фармаколошким својствима, индикацијама за употребу и нежељеним ефектима терапије за сваку од ових група лекова.
Индикације за употребу типичних антипсихотика
Тренутно, главне индикације за прописивање традиционалних неуролептика, према препорукама ауторитативних истраживача у области психофармакотерапије, укључују следеће.
- Ублажавање психомоторне агитације и поремећаја понашања изазваних тешким психотичним симптомима. У овим случајевима је индикована употреба оралних или парентералних облика лекова са антипсихотичним дејством, како глобалних (клопромазин, левомепромазин, тиопроперазин, зуклопентиксол) тако и селективних - у облику дејства на халуцинаторно-параноидне поремећаје (халоперидол, трифлуоперазин).
- Антирецидивна (превентивна) терапија. У ту сврху се прописују депо облици лекова, посебно код пацијената са лошом компатибилношћу са лековима (халоперидол деканоат, продужени облик флупентиксола), или мале или средње дозе лекова за добијање дезинхибиторног (антинегативног) ефекта, из редова оних лекова чије се високе дозе користе за ублажавање акутних психотичних поремећаја (флупентиксол, зуклопентиксол). Код ове врсте терапије препоручује се и прописивање такозваних малих неуролептика (тиоридазин, хлорпротиксен, сулпирид), чија се психотропна активност састоји у дејству на манифестације депресивног пола и поремећаје несанице.
- Превазилажење терапијске резистенције на атипичне антипсихотике у лечењу акутних психотичних стања. У ту сврху се обично користе парентерални облици традиционалних антипсихотика са глобалним (хлорпромазин, левомепромазин итд.) и селективним (халоперидол) антипсихотичним дејством.
Ови лекови изазивају различите нежељене ефекте, чија природа зависи од карактеристика фармаколошког профила сваког лека. Антипсихотици са израженијим холинолитичким ефектом чешће изазивају поремећаје акомодације, затвор, сува уста и задржавање урина. Седативни ефекат је типичнији за антипсихотике са израженим антихистаминским ефектом, а ортостатска хипотензија је типичнија за лекове који блокирају α1-адренергичке рецепторе. Блокада холинергичке, нордренергичке и допаминергичке трансмисије типичним неуролептицима може довести до низа поремећаја у сексуалној сфери, као што су аменореја или дисменореја, аноргазмија, галактореја, оток и бол у млечним жлездама и смањена потенција. Нежељени ефекти у сексуалној сфери су углавном повезани са холинолитичким и адреноблокирајућим својствима ових лекова, а такође и са повећањем секреције пролактина услед блокаде метаболизма допамина. Најозбиљнији нежељени ефекти типичних неуролептика су моторна дисфункција. Они су најчешћи разлог због којег пацијенти престају да узимају лекове. Три главна нежељена ефекта терапије повезана са утицајем на моторичку сферу укључују ране екстрапирамидалне синдроме, тардивну дискинезију и НМС.
Верује се да су екстрапирамидални синдроми повезани са блокадом D2 рецептора у базалним ганглијама. Они укључују дистонију, неуролептички паркинсонизам и акатизију. Манифестације акутне дистоничне реакције (рана дискинезија) укључују изненада насталу хиперкинезу, окулогирне кризе, контракције мишића лица и трупа, опистотонус. Ови поремећаји зависе од дозе и често се јављају након 2-5 дана терапије веома потентним неуролептицима као што су халоперидол и флуфеназин. Да би се ублажила рана дискинезија, доза неуролептика се смањује и прописују се антихолинергички лекови (бипериден, трихексифенидил). Тардивна дискинезија обично захвата мишиће врата и, за разлику од акутне дистоничне реакције, мање реагује на лечење антихолинергичким лековима. Неуролептички паркинсонизам карактерише смањење спонтане моторике, хипо- и амимија, тремор у мировању и ригидност. Важно је разликовати ове симптоме од споља сличних негативних поремећаја код шизофреније, који се испољавају емоционалном отуђеношћу, притупљењем афекта и анергијом. За корекцију ових нежељених ефеката индикована је употреба антихолинергика, смањење дозе неуролептика или његова замена атипичним антипсихотиком. Акатизија се манифестује унутрашњом анксиозношћу, немогућношћу дужег остајања на једном месту и потребом за сталним померањем руку или ногу. За њено ублажавање користе се антихолинергици и централни бета-блокатори (пропранолол).
Касна дискинезија се манифестује невољним покретима било које мишићне групе, најчешће мишића језика и уста. Клинички се разликује неколико њених облика: дискинезија мишића образа, језика, уста (периодични грчеви жвакаћих мишића, стварајући утисак особе која прави гримасу, језик може невољно вирити из уста пацијента); тардивна дистонија и тардивна акатизија; (пацијент прави хореоатетоидне покрете главом, трупом, горњим и доњим удовима). Овај облик поремећаја се бележи углавном током дуготрајног лечења традиционалним неуролептицима и открива се код приближно 15-20% пацијената који их узимају као терапију одржавања. Вероватно је код неких пацијената повећан ризик од развоја симптома дискинезије, пошто су неки од њих примећени у клиници шизофреније чак и пре „неуролептичке ере“. Поред тога, тардивна дискинезија је описана код старијих жена и пацијената са афективним поремећајима. Сматра се да је тардивна дискинезија повезана са повећањем броја допаминских рецептора у стријатуму, иако је вероватно да су ГАБАергички и други неуротрансмитерски системи такође укључени у њену патогенезу. Не постоји ефикасан универзални третман за такве нежељене ефекте. Сугерише се да ниске дозе високо потентних неуролептика са дејством блокирања допамина или витамина Е могу имати умерен благотворан ефекат код ових поремећаја. Најефикаснија мера за тардивну дискинезију је смањење дозе типичног неуролептика или његова замена атипичним антипсихотиком.
Према тренутним подацима, неуролептички малигни синдром се јавља у приближно 0,5% случајева психофармакотерапије. Вероватно се ретка појава ове животно угрожавајуће компликације тренутно може објаснити широко распрострањеном применом атипичних антипсихотика у праксу, будући да је ризик од развоја НМС-а током лечења овим лековима незнатан. Општеприхваћено је да је главни узрок развоја НМС-а прекомерна блокада допаминергичког система током терапије неуролептицима, посебно након повећања дозе високо потентног антипсихотика. Главни симптоми НМС-а су хипертермија, повећан тонус скелетних мишића и тетивних рефлекса, оштећена свест са преласком у кому. Анализе крви откривају леукоцитозу, повећану брзину седиментације еритроцита, активност јетрених трансаминаза; анализе урина откривају присуство албуминурије. Поремећаји равнотеже воде и електролита се брзо јављају, што ствара предуслове за формирање церебралног едема. НМС је акутно стање које захтева хитну хоспитализацију пацијента ради интензивне инфузионе терапије. У лечењу НМС-а, хидратација и симптоматска терапија су најважније. У овој ситуацији, сваки прописани неуролептик захтева хитан прекид употребе. У неким случајевима, агонисти допаминских рецептора (на пример, бромокриптин) или мишићни релаксанти имају позитиван ефекат, иако њихова ефикасност није проучавана. Након елиминације НМС-а, неуролептик не треба поново узимати најмање две недеље. Након тога, може се прописати антипсихотик мале јачине, пожељно лек нове генерације. Дозу новопрописаног лека треба изузетно пажљиво повећавати, пратећи стање виталних функција и лабораторијске податке (тестови крви и урина).
Типични неуролептици ретко изазивају опасне фаталне компликације. Манифестације предозирања су углавном повезане са индивидуалним профилом антиадренергичког и антихолинергичког дејства лека. Пошто ови лекови имају јак антиеметик, индицирано је испирање желуца за њихово елиминисање из организма, а не примена еметика. Артеријска хипотензија је, по правилу, последица блокаде адренергичких рецептора и треба је кориговати применом допамина и норепинефрина. У случају срчане аритмије, индикована је употреба лидокаина.
Механизам деловања и фармаколошки ефекти типичних антипсихотика
Како се психофармакологија развијала, предложене су различите опције за дејство антипсихотика на неурорецепторе. Главна хипотеза остаје да они утичу на допаминске неуроструктуре (првенствено D2 рецепторе), на основу података о поремећају нормалног метаболизма допамина у можданим структурама код психоза. Допамински D2 рецептори се налазе у базалним ганглијама, nucleus accumbens-у и фронталном кортексу; они играју водећу улогу у регулацији протока информација између мождане коре и таламуса.
Слика показује детаљније разумевање поремећаја у преносу допамина у кортикалним и субкортикалним областима мозга и улоге ових поремећаја у развоју симптома шизофреније (адаптирано из монографије аутора Jones RB, Buckley PF, 2006).
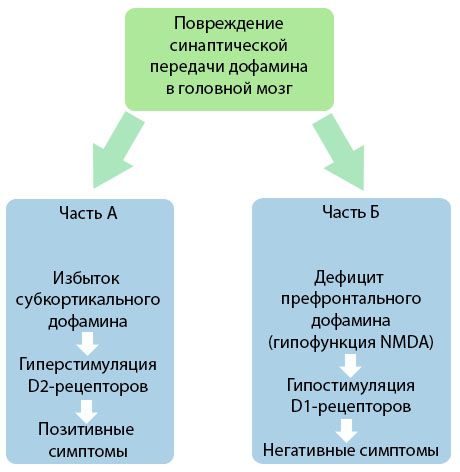
Део А одражава класичну, рану допамински теорију, постулирајући вишак допамина у субкортикалним областима и хиперстимулацију Д2 рецептора, што доводи до појаве продуктивних симптома. Део Б демонстрира накнадну модернизацију теорије почетком 1990-их. Подаци добијени до тада открили су да недостатак допамина у Д рецепторима, заједно са недовољном стимулацијом ових рецептора у префронталном кортексу, доводи до појаве негативних симптома и когнитивних дефицита. Стога, према савременом схватању, обе врсте поремећаја допаминергичке трансмисије - вишак субкортикалног допамина и његов недостатак у префронталном кортексу - су комбиновани резултат поремећаја синаптичке трансмисије у префронталној области и повезани су са хипофункцијом Н-метил-Н-аспартата. Поред првобитно изолованог допамина, касније су идентификовани и други неуротрансмитери укључени у патогенезу шизофреније, као што су серотонин, гама-аминобутерична киселина, глутамат, норепинефрин, ацетилхолин и различити неуропептиди. Иако улога ових медијатора није у потпуности проучена, ипак, како се знање развија, постаје јасно да је манифестација бројних неурохемијских помака у телу. Стога, клинички ефекат антипсихотичног лека је збир ефеката на различите рецепторске формације и доводи до елиминације поремећаја хомеостазе.
Последњих година, захваљујући појави нових истраживачких метода као што су везивање радиоизотопских лиганда и ПЕТ скенирање, постигнут је значајан напредак у разјашњавању финог биохемијског механизма деловања неуролептика. Посебно је утврђена упоредна снага и тропизам лекова да се вежу за појединачне неурорецепторе у различитим областима и структурама мозга. Показана је директна зависност тежине антипсихотичног дејства лека од јачине његовог блокирајућег дејства на различите допаминергичке рецепторе. Недавно су идентификоване четири врсте таквих рецептора:
- Д1 се налазе претежно у пределу супстанције нигре и стријатума (тзв. нигростријатална регија), као и префронталне регије;
- Д2 - у нигростријаталним, мезолимбичним регионима и предњем режњу хипофизе (секреција пролактина);
- Д3 (пресинаптички) - у различитим можданим структурама, контролишу допаминергичку активност према закону негативне повратне спреге;
- Д4 (пресинаптички) - претежно у нигростријаталним и мезолимбичким областима.
Истовремено, сада се може сматрати доказаним да је управо блокада D2 рецептора узрок развоја антипсихотичних, секундарних седативних ефеката, као и екстрапирамидалних нежељених ефеката. Друге клиничке манифестације блокаде ове врсте рецептора су аналгетички и антиеметички ефекат неуролептика (смањење мучнине, повраћања као резултат супресије центра за повраћање), као и смањење садржаја хормона раста и повећање производње пролактина (неуроендокрини нежељени ефекти, укључујући галактореју и менструалне неправилности). Дуготрајна блокада нигростријаталних D2 рецептора доводи до појаве њихове преосетљивости, што је одговорно за развој тардивних дискинезија и „психоза преосетљивости“. Вероватне клиничке манифестације блокаде пресинаптичких D3 и D4 рецептора повезане су углавном са стимулативним дејством неуролептика. Због делимичне блокаде ових рецептора у нигростријаталним и мезолимбокортикалним областима, активирајући и инцизивни (снажни, високо активни) неуролептици у малим дозама могу стимулисати, а у високим дозама сузбити допаминергички пренос.
Последњих година, интересовање за функцију серотонергичких система мозга, укључујући серотонинске рецепторе, нагло је порасло. Чињеница је да у различитим деловима мозга серотонергички систем има модулирајући ефекат на допаминергичке структуре. Конкретно, у мезокортикалној регији, серотонин инхибира ослобађање допамина, и сходно томе, блокада постсинаптичких 5-HT рецептора доводи до повећања садржаја допамина. Као што је познато, развој негативних симптома код шизофреније повезан је са хипофункцијом допаминских неурона у префронталним структурама мождане коре. Тренутно је познато око 15 врста централних 5-HT рецептора. Експериментално је откривено да се неуролептици везују углавном за 5-HT рецепторе прва три типа.
Ови лекови имају претежно стимулативни (агонистички) ефекат на 5-HT1a рецепторе. Вероватне клиничке последице: повећана антипсихотична активност, смањена тежина когнитивних поремећаја, корекција негативних симптома, антидепресивни ефекат и смањена учесталост екстрапирамидалних нежељених ефеката.
Дејство неуролептика на 5-HT2 рецепторе, посебно на 5-HT2a подтипове, је од значајног значаја. Они се налазе углавном у можданој кори и њихова осетљивост је повећана код пацијената са шизофренијом. Способност неуролептика нове генерације да смање тежину негативних симптома, побољшају когнитивне функције, регулишу сан повећањем укупног трајања спороталасних (D-таласних) фаза спавања, смање агресију и ублаже депресивне симптоме и главобоље сличне мигрени (које настају услед цереброваскуларних поремећаја) повезана је са блокадом 5-HT2a рецептора. С друге стране, блокадом 5-HT2a рецептора могући су хипотензивни ефекти и поремећаји ејакулације код мушкараца.
Верује се да ефекат неуролептика на 5-ХТ2ц рецепторе изазива седативни (анксиолитички) ефекат, повећан апетит (праћен повећањем телесне тежине) и смањење производње пролактина.
5-HT3 рецептори се налазе претежно у лимбичком региону, и када су блокирани, прво се развија антиеметичко дејство, а појачавају се и антипсихотично и анксиолитичко дејство.
Појава симптома сличних Паркинсонизму такође зависи од блокирајуће моћи лека на мускаринске холинергичке рецепторе. Холинолитички и допамински блокирајући ефекти су донекле у реципрочним односима. Познато је, на пример, да у нигростријаталној регији Д2 рецептори инхибирају ослобађање ацетилхолина. Када је блокирано више од 75% Д2 рецептора у нигростријаталној регији, равнотежа је поремећена у корист холинергичког система. То је разлог корективног дејства антихолинергичких лекова (коректора) на неуролептичке екстрапирамидалне нежељене ефекте. Хлорпротиксен, клозапин и оланзапин имају висок афинитет за мускаринске рецепторе и практично не изазивају екстрапирамидалне нежељене ефекте, пошто истовремено блокирају холинергичке и допаминергичке рецепторе. Халоперидол и пиперазин фенотиазински деривати имају изражен ефекат на допаминске рецепторе, али имају веома слаб ефекат на холинске рецепторе. То је због њихове способности да изазову изражене екстрапирамидалне нежељене ефекте, који се смањују када се користе веома високе дозе, када холинолитички ефекат постаје приметан. Поред смањења ефекта блокирања допамина на Д2 рецепторе нигростријаталне регије и изравнавања екстрапирамидалних нежељених ефеката, јак холинергички ефекат може изазвати погоршање когнитивних функција, укључујући поремећаје памћења, као и периферне нежељене ефекте (суве слузокоже, оштећена визуелна акомодација, затвор, задржавање урина, конфузија итд.). Неуролептици имају прилично јак блокирајући ефекат на хистаминске рецепторе типа I, што је повезано, пре свега, са тежином седативног ефекта, као и са повећањем телесне тежине услед повећаног апетита. Антиалергијски и антипруритични ефекти неуролептика такође су повезани са њиховим антихистаминским својствима.
Поред блокирања допамина, антисеротонергичког, холинолитичког и антихистаминског дејства, већина неуролептика има адренолитичка својства, односно блокирају и централне и периферне α1-адренорецепторе. Адреноблокатори попут хлорпромазина и хлорпротиксена имају изражен седативни ефекат. Поред тога, блокирајући ефекат ових лекова може изазвати неуровегетативне нежељене ефекте (артеријску хипотензију, тахикардију итд.), као и повећање хипотензивног ефекта адреноблокатора.
Радови великог броја аутора пружају податке о јачини везивања (афинитету) појединачних неуролептика са различитим типовима неурорецептора.
На основу свог неурохемијског профила деловања, типични и атипични антипсихотици, међу онима који се претежно користе у клиничкој пракси, могу се условно поделити у шест група.
Прву групу чине селективни блокатори Д2 и Д4 рецептора (сулпирид, амисудприд, халоперидол, итд.) из група деривата бензамида и бутирофенона. У малим дозама, углавном због блокаде пресинаптичких Д4 рецептора, активирају допаминергички пренос нервних импулса и имају стимулативни (дезинхибиторни) ефекат, у великим дозама блокирају Д2 рецепторе у свим областима мозга, што се клинички манифестује израженим антипсихотичким ефектом, као и екстрапирамидалним и ендокриним (због пролактинемије) нежељеним ефектима.
Друга група обухвата високо активне блокаторе Д2-рецептора, као и лекове који слабо или умерено блокирају 5-ХТ2а- и 5-ХТ1а-рецепторе (флупентиксол, флуфеназин, зуклопентиксол итд.), односно углавном пиперазинске деривате фенотиазина или тиоксантене блиске њима по стереохемијској структури. Као и лекови прве групе, ови неуролептици имају, пре свега, изражен антипсихотични (инцизивни) ефекат, а такође изазивају екстрапирамидалне пие ефекте и пролактинемију. У малим дозама имају умерено активирајући (психостимулирајући) ефекат.
Трећу групу чине поливалентни седативни неуролептици који блокирају већину неурорецептора на недиференциран начин. Ови лекови имају јасно изражен блокирајући ефекат на допаминске рецепторе, а такође изазивају јаке адренолитичке и холинолитичке ефекте. Ово укључује већину седативних неуролептика, пре свега алифатичне и пиперидински деривате фенотиазина, као и тиоксантене који су им блиски по стереохемијској структури (хлорпромазин, левомепромазин, хлорпротиксен, итд.). Спектар психотропне активности ових лекова доминира, пре свега, израженим примарним седативним ефектом, који се развија без обзира на примењену дозу, и умереним антипсихотичним ефектом. Поред тога, због свог израженог антихолинергичког ефекта, лекови ове групе изазивају слабе или умерене екстрапирамидалне и неуроендокрине нежељене ефекте, али често доводе до развоја ортостатске хипотензије и других аутономних реакција услед изражене блокаде α1-адренергичких рецептора.
Четврта група обухвата неуролептике који блокирају D2- и 5-HT2a-рецепторе на уравнотежен начин, односно у истој мери (ови последњи у нешто већој мери) и a1-адренорецепторе у умереној мери. Ова група обухвата представнике нове генерације атипичних антипсихотика (рисперидон, зипрасидон, сертиндол), који имају различите хемијске структуре. Неурохемијски механизам деловања одређује њихов селективни утицај првенствено на мезолимбичке и мезокортикалне области мозга. Уз изразит антипсихотички ефекат, одсуство или слабу израженост екстрапирамидалних нежељених ефеката (при примени терапијских доза), слабу или умерену пролактинемију и умерена адренолитичка својства (хипотензивне реакције), ова група неуролептика је у стању да коригује негативне симптоме индиректном стимулацијом допаминергичке трансмисије у можданој кори.
Пету групу чине поливалентни атипични антипсихотици трицикличног дибензодиазепина или сличне структуре (клозапин, оланзапин и кветиапин). Баш као и лекови треће групе, они блокирају већину неурорецептора на недиференциран начин. Међутим, 5-ХТ2а рецептори су блокирани јаче од Д2 и Д4 рецептора, посебно оних који се налазе у нигростријаталној регији. Ово одређује стварно одсуство или слабо екстрапирамидално дејство и одсуство неуроендокриних нежељених ефеката повезаних са повећаном производњом пролактина са израженим антипсихотичким дејством и способношћу смањења тежине негативних симптома. Поред тога, сви лекови ове групе имају изражена адренолитичка и антихистаминска својства, што одређује седативне и хипотензивне ефекте. Клозапин и оланзапин такође имају прилично изражен блокирајући ефекат на мускаринске рецепторе и доводе до развоја холинолитичких нежељених ефеката.
Дакле, способност блокирања постсинаптичких допаминергичких рецептора са компензаторним повећањем синтезе и метаболизма допамина је једино заједничко биохемијско својство за све неуролептике који се разматрају у овим групама.
Шеста група обухвата једини атипични антипсихотик, арипипразол, који се релативно недавно појавио на домаћем психофармаколошком тржишту. Овај лек је делимични агонист Д2-допаминских рецептора, и делује као функционални антагонист у хипердопаминергичком стању и као функционални агонист у хиподопаминергичком профилу. Такав јединствени рецепторски профил арипипразола омогућава смањење ризика од екстрапирамидалних поремећаја и хиперпролактинемије приликом његове употребе. Поред тога, арипипразол делује као делимични агонист 5-HT1a рецептора и истовремено је антагонист 5-HT2a рецептора. Претпоставља се да таква интеракција са рецепторима доводи до генерално уравнотеженог функционисања серотонинског и допаминског система, па се механизам деловања арипипразола може означити као стабилизација допамин-серотонинског система.
Дакле, тренутни ниво знања о неурохемијским механизмима деловања неуролептика нам омогућава да предложимо нову, патогенетски поткрепљенију фармакодинамичку класификацију ове групе психотропних лекова. Употреба ове класификације нам омогућава да у великој мери предвидимо спектар психотропне активности, толеранцију и вероватне интеракције лекова одређеног лека. Другим речима, карактеристике неурохемијске активности лека у великој мери одређују карактеристике његове клиничке активности, што треба користити при избору одређеног антипсихотичног лека за конкретног пацијента.
Ефикасност глобалног антипсихотичног ефекта било ког неуролептика процењује се коришћењем такозваног хлорпромазинског еквивалента, који се узима као 1. На пример, хлорпромазински еквивалент халоперидола = 50. То значи да је антипсихотичка ефикасност 1 мг халоперидола упоредива са 50 мг хлорпромазина. На основу овог индикатора развијена је класификација која предвиђа раздвајање неуролептика са високом (хлорпромазински еквивалент > 10,0), средњом (хлорпромазински еквивалент = 1,0-10,0) и ниском (хлорпромазински еквивалент = 1,0) антипсихотском активношћу, названом патентност. Типични неуролептици (антипсихотици прве генерације) се широко користе у клиничкој психофармакотерапији скоро пола века. Спектар њихове терапијске активности обухвата:
- глобално антипсихотично дејство у облику способности равномерног и диференцијалног смањења различитих манифестација психозе:
- примарни седативни (инхибиторни) ефекат - способност лекова да брзо ублаже психомоторну агитацију;
- селективно, селективно антипсихотично дејство, које се манифестује у способности утицаја на појединачне симптоме: делиријум, халуцинације, дезинхибиција нагона итд.;
- активирајуће (дезинхибиторно, дезинхибиторно, антиаутистично) неуротропно дејство, које се манифестује развојем екстрапирамидалних симптома;
- соматотропно дејство у облику развоја неуроендокриних и вегетативних нежељених ефеката;
- депресивни ефекат, изражен у способности неких антипсихотика да изазову депресивне симптоме.
Ефикасност антипсихотика прве генерације у лечењу не само психотичних поремећаја, већ и поремећаја у оквиру граничне психијатрије је више пута доказана и неспорна је. Стога, упркос високој учесталости нежељених ефеката терапије када се прописују, они се и даље користе у медицинској пракси.
Атипични антипсихотици
Савремене смернице садрже податке о предностима коришћења антипсихотика друге генерације у фармакотерапији. Термин „атипични“ (синоним - антипсихотици друге генерације) је услован и користи се углавном због погодности означавања нове генерације. У поређењу са традиционалним неуролептицима, лекови ове групе су ефикаснији у корекцији негативних, афективних и когнитивних поремећаја, што је комбиновано са бољом подношљивошћу и мањим ризиком од екстрапирамидалних симптома. Разлике у природи терапијског дејства једног или другог лека из низа атипичних антипсихотика објашњавају се, као и код групе типичних неуролептика, његовим индивидуалним профилом фармаколошког дејства.
Да би се разјасниле могућности психофармакотерапије атипичним антипсихотицима, препоручљиво је фокусирати се на лекове ове групе регистроване у Русији.
 [ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
[ 28 ], [ 29 ], [ 30 ], [ 31 ], [ 32 ], [ 33 ]
Клозапин (дибензодиазепин)
Оснивач групе атипичних антипсихотика. Механизам деловања клозапина карактерише се благом блокадом D2 рецептора уз истовремени висок антагонизам према 5-HT2a рецепторима, a1, a2-адренергичким и H1-хистаминским рецепторима. Доказао се као ефикасан антипсихотик у случајевима резистенције на друге антипсихотике (лек резервне групе), а такође је индикован за лечење хроничне маније, психотичне агитације, агресије. У домаћој пракси, клозапин се често прописује за постизање седације и као хипнотик код психотичних пацијената. Треба признати да таква употреба клозапина не одговара његовом главном профилу индикација за употребу у терапији. Вероватно би став према овом антипсихотику као леку секундарног значаја требало ревидирати, јер је данас то једини лек са доказаном ефикасношћу код резистентних пацијената.
Клозапин, за разлику од типичних неуролептика, не изазива озбиљне екстрапирамидалне поремећаје због поменутог ниског афинитета за О2 рецепторе. Такође се испоставило да се може користити за лечење касне дистоније и тешке акатизије. Због ниског ризика од развоја НМС-а, клозапин се може сматрати леком избора код пацијената који су претходно патили од ове компликације.
Међутим, током терапије клозапином може се развити низ озбиљних нежељених ефеката. Најопаснији од њих (чак и када се прописују мале дозе) је агранулоцитоза, која се јавља код 0,5-1,0% пацијената. Други важни нежељени ефекти који се могу јавити приликом употребе лека укључују поспаност, хиперсаливацију и повећање телесне тежине, која је често већ повишена до тренутка када се клозапин прописује под утицајем претходне антипсихотичке терапије. Такође треба обратити пажњу на могућност развоја тахикардије, артеријске хипотензије и епилептичних нападаја приликом узимања. Вероватноћа нападаја зависи од дозе. Њихов ризик се значајно повећава ако доза клозапина пређе 600 мг/дан. Развој нападаја није контраиндикација за даљу употребу лека, али захтева преполовљење дозе и прописивање антиконвулзива, као што је валпроинска киселина. Превенција нежељених ефеката лечења клозапином укључује пажљиво праћење броја белих крвних зрнаца, као и ЕКГ и ендокриних параметара.
Предозирање клозапином може изазвати депресију свести до развоја коме, као и симптоме повезане са холинолитичким ефектом (тахикардија, делиријум), епилептичке нападе, респираторну депресију, екстрапирамидалне синдроме. Смртни исход може настати када се узима доза већа од 2500 мг лека.
 [ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
[ 34 ], [ 35 ], [ 36 ], [ 37 ], [ 38 ], [ 39 ], [ 40 ], [ 41 ]
Рисперидон
Дериват бензизоксазола са високим афинитетом за серотонинске и допаминске Dj рецепторе са претежним дејством на серотонински систем. Лек има широк спектар индикација за употребу, укључујући ублажавање егзацербација, лечење против рецидива, терапију за прву психотичну епизоду и корекцију негативних симптома шизофреније. Показано је да лек побољшава когнитивне функције код пацијената са шизофренијом. Добијени су прелиминарни подаци да рисперидон такође смањује коморбидне афективне симптоме код пацијената са шизофренијом и да може бити лек избора у лечењу биполарних афективних поремећаја.
Нежељени ефекти терапије рисперидоном, посебно екстрапирамидални поремећаји, зависе од дозе и јављају се чешће у дозама које прелазе 6 мг/дан. Остали нежељени ефекти укључују мучнину, повраћање, анксиозност, поспаност и повећање нивоа пролактина у серуму. Дуготрајна употреба рисперидона може довести до повећања телесне тежине и развоја дијабетес мелитуса типа 2, али са мањом вероватноћом у поређењу са клозапином, оланзапином.
Предозирање може изазвати поспаност, епилептичке нападе, продужење QT интервала и проширење QRS комплекса, као и артеријску хипотензију. Описани су случајеви смртног исхода услед предозирања рисперидоном.
Несумњива предност лека је доступност течних и брзорастворљивих (сублингвалних) облика, чија употреба убрзава улазак лека у организам пацијента и олакшава контролу над његовим уносом. Постоји и продужени облик лека - прашак за припрему суспензије за интрамускуларну примену (конста-рисперидон у микросферама). Препоручује се за одржавајућу терапију пацијената са шизофренијом, посебно за пацијенте са лошом комплајнсом. Потребно је узети у обзир чињеницу да је леку потребно око три недеље да уђе у крвоток, стога, приликом започињања терапије конста-рисперидоном, пацијент мора додатно узимати орални облик рисперидона најмање 3 недеље након прве ињекције.
Оланзапин
По фармаколошком дејству, близак је клозапину, јер има плеиоморфни рецепторски профил са значајним афинитетом за серотонинске, мускаринске, α1-адренергичке и хистаминске рецепторе. Терапеутска активност оланзапина има карактеристике сличне ефикасности клозапина и рисперидона у погледу утицаја на позитивне, негативне и депресивне симптоме шизофреније. Истовремено, добијени су подаци о већој ефикасности оланзапина у поређењу са другим атипичним антипсихотицима код пацијената са првом психотичном епизодом и у корекцији показатеља когнитивног функционисања. Треба узети у обзир да се на почетку терапије применом таблетног облика лека може јавити брз дезинхибиторни ефекат са повећаном психомоторном агитацијом и анксиозношћу. Стога је у лечењу напада праћених тешком психомоторном агитацијом индикована употреба ињекционог облика лека.
Оланзапин ретко изазива екстрапирамидалне поремећаје или тардивну дискинезију, а најчешћи нежељени ефекти код његове употребе су метаболички поремећаји и повећање телесне тежине. Утврђено је да пацијенти који примају оланзапин прилично често доживљавају повишен ниво холестерола, липида у плазми и предиспозицију за дијабетес мелитус типа 2, али такви ефекти су били подједнако чести код пацијената који су примали и оланзапин и клозапин. Истовремено, добијени су подаци који показују да повећање телесне тежине корелира са позитивним одговором на оланзапин (тј. служи као важан прогностички индикатор терапије), а развија се у гојазност само код 20-30% пацијената који су добили вишак килограма током лечења.
Предозирање може изазвати седацију, токсичне антихолинергичке ефекте, епилептичке нападе и артеријску хипотензију. Тренутно нема убедљивих података за процену ризика од смрти услед предозирања.
Кветиапин
Класификован је као дибензотиазепинско једињење. Његов рецепторски профил је у великој мери сличан профилу клозапина. Ниво везивања кветиапина за Д2 рецепторе је низак (мање од 50%) и краткотрајан чак и када се користе високе дозе. Лек је ефикасан у лечењу позитивних, негативних и општих симптома шизофреније. Постоје докази о његовој успешној употреби како у случајевима високе отпорности на терапију, тако и за побољшање когнитивног функционисања пацијената, што даје право да се препоручи као антипсихотик прве линије за одржавајућу терапију шизофреније. Коначно, кветиапин има умерено антидепресивно, активирајуће дејство. Стога је индикован у лечењу депресивно-делузионих напада и поремећаја сенесто-хипохондријског круга.
Утврђена висока тимотропна активност кветиапина објашњава чињеницу да је регистрован као средство за ублажавање и секундарну превенцију депресивних поремећаја. За лечење маничних епизода у оквиру биполарних поремећаја типа I и II, кветиапин се користи као додатно средство. Одсуство ињекционих облика донекле ограничава његову употребу код пацијената са агитацијом и агресивним понашањем.
Кветиапин се добро подноси, практично не изазива екстрапирамидалне синдроме, осим у случајевима када се користе максималне дозе. Кветиапин не изазива хиперпролактинемију, ређе од оланзапина и клозапина, доводи до повећања телесне тежине и поремећене толеранције на глукозу.
Зипрасидон
Има јединствен профил рецепторске активности. Као снажан антагонист 5HT2a рецептора и D2 рецептора, такође је активни инхибитор поновног преузимања серотонина и норепинефрина. Клиничке студије су показале значајну супериорност зипрасидона у његовом дејству на психотичне симптоме и манифестације агресије у поређењу са халоперидолом. Такође постоје подаци о позитивном дејству зипрасидона на когнитивне функције пацијената са шизофренијом, као и на коморбидне афективне симптоме, индикаторе социјалног функционисања. Зипрасидон се обично добро подноси и веома ретко изазива екстрапирамидалне синдроме, повећање телесне тежине и метаболичке поремећаје. Чешће долази до продужења QT интервала преко 460 ms, стога је препоручљиво да пацијенти који примају овај лек прођу ЕКГ преглед и пре прописивања лека и контролно праћење током лечења. Посебну пажњу треба обратити на истовремену терапију (узимање антиаритмичких лекова), која може погоршати продужење QT интервала и довести до развоја срчане аритмије, вентрикуларне фибрилације.
Сертиндол
Припада дериватима фенилиндола. Има висок функционални антагонизам у односу на Д2-, серотонин (посебно 5-ХТ2а-рецепторе) и α1-адренергичке рецепторе. Према електронеурохемијским студијама, сертиндол селективно инхибира допаминске рецепторе у вентралном сегментном региону. Таква селективност, по свој прилици, обезбеђује низак ризик од екстрапирамидалних синдрома и хиперпролактинемије при употреби лека. Резултати упоредних студија показали су да је сертиндол упоредив са халоперидолом у погледу антипсихотичке активности. Лек има изражен дезинхибиторни ефекат код пацијената са негативним и депресивним симптомима, који је супериорнији у односу на сличан ефекат рисполепта. Такође постоје докази који потврђују ефикасност сертиндола за корекцију когнитивног оштећења код пацијената са шизофренијом. Сертиндол генерално добро подносе пацијенти, ретко изазива седацију и стога се препоручује као заменски лек када се нежељени ефекти јаве током терапије другим савременим антипсихотицима.
Озбиљни нежељени ефекти укључују способност лека да продужи QT интервал, што може довести до срчане аритмије. Приликом анализе постмаркетиншких студија, постало је јасно да се срчани профил сертиндола не разликује од профила других антипсихотика нове генерације.
Арипипразол
Има антипсихотичну активност упоредиву са другим атипичним агенсима, али има већи ефекат на параметре когнитивног функционисања пацијената са шизофренијом. Горе поменуто јединствено фармаколошко дејство лека - делимични агонист Д2 рецептора - омогућава смањење ризика од екстрапирамидалних синдрома и хиперпролактинемије приликом његове употребе.
 [ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
[ 42 ], [ 43 ], [ 44 ], [ 45 ], [ 46 ], [ 47 ]
Амисулприд
Припада класи супституисаних бензамида. Лек се селективно везује за подтипове D2 и D3 допаминергичких рецептора, нема афинитет за подтипове D1, D4 и D5, као ни за серотонин, H1-хистаминске, a1-адренергичке и холинергичке рецепторе. Када се користи у високим дозама, блокира постсинаптичке D2 рецепторе. У ниским дозама, његов дезинхибиторни ефекат се манифестује услед блокаде пресинаптичких D2, D3 рецептора, због чега је његова употреба ефикасна и у лечењу негативних симптома, иако није комбиновани антагонист D2 рецептора и серотонинских рецептора. Резултати бројних студија указују на изражену антипсихотску активност лека када се користи у високим дозама, која је супериорнија у односу на традиционалне лекове.
 [ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
[ 48 ], [ 49 ], [ 50 ], [ 51 ], [ 52 ], [ 53 ], [ 54 ], [ 55 ]
Нежељени ефекти антипсихотичке терапије
Табела наводи главне нежељене ефекте атипичне антипсихотичке терапије.
Припрема |
Екстрапирамидални |
Поремећај проводљивости на ЕКГ-у |
Метаболички поремећаји (повећање телесне тежине, повећање нивоа глукозе, холестерола, триглицерида у крви) |
||
Клозапин |
. |
++ |
++ |
++- |
|
Рисперидон |
++ |
+/- |
++ |
+/- |
|
Оланзапин |
+ |
+/- |
+++ |
++ |
+++ |
Кветиапин |
+/- |
+ |
+/- |
--- |
|
Зипрасидон |
+ |
++ |
+/- |
+/- |
+/- |
Сертиндол |
++ |
-- |
+/- |
-- |
|
Арилипразол |
-- |
--- |
+/- |
-- |
-- |
Амисулприд |
++ |
+/- |
|||
Напомена. Тежина нежељених ефеката: "+++" - висока; "++" - просечна; "+" - ниска; "+/-" - сумњива; "-" - одсутна.
Екстрапирамидални синдроми
Једна од главних карактеристика атипичних антипсихотика, за разлику од традиционалних, је њихова ниска способност да изазову екстрапирамидалне синдроме, што је постало пробој у фармакотерапији одржавања шизофреније. Међутим, као што следи из података у табели, приликом употребе појединачних лекова ове серије (рисперидон, амисулприд) могу се јавити такви симптоми, што захтева посебну пажњу приликом њиховог прописивања.
 [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
ЕКГ абнормалности
Могућност развоја кардијалних нежељених ефеката је озбиљан проблем при коришћењу неких савремених антипсихотика у терапији. У овим случајевима говоримо о продужењу QT интервала, што може довести до развоја аритмије. Поремећаји проводљивости, пре свега продужење QT интервала, најчешће се примећују током лечења клозапином, сертиндолом, зипрасидоном. Истовремена патологија у облику брадикардије, атриовентрикуларног блока, хипотиреоидизма може допринети појави ове компликације током терапије горе поменутим лековима. Тренутно се препоручује ЕКГ праћење приближно једном на свака 3 месеца код пацијената који примају терапију одржавања атипичним антипсихотицима.
 [ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
[ 11 ], [ 12 ], [ 13 ], [ 14 ], [ 15 ]
Ендокрини поремећаји
Тренутно, највећу забринутост изазива способност атипичних антипсихотика да изазову повећање телесне тежине. Повећана телесна тежина, ниво глукозе и триглицерида у крви могу довести до метаболичких поремећаја и развоја дијабетеса типа 2. Посебан опрез и недељно праћење биохемијских параметара су неопходни током терапије клозапином и оланзапином. Према мишљењу J. Geddes et al. (2000), PB Jones, PF Buckley (2006), требало би препознати као прикладно спровести темељан преглед пацијената пре него што им се пропише одређени антипсихотик модерне генерације, будући да је познато да се метаболички поремећаји чешће јављају код пацијената који су имали наследну предиспозицију, прекомерну телесну тежину, поремећаје липидног спектра и хипергликемију пре почетка лечења. Алгоритам праћења који су предложили PB Jones, PF Buckley (2006) укључује неколико тачака.
- Прикупљање медицинске историје и породичних фактора у вези са ризиком од метаболичких поремећаја.
- Регистрација индекса телесне масе, ЕКГ-а, крвног притиска и пулса пре почетка лечења.
- Прикупљање лабораторијских података (глукоза, липидни профил, холестерол) пре почетка терапије.
- Редовно праћење индекса телесне масе и виталних знакова током лечења.
- Праћење лабораторијских података током лечења.
Појава хиперпролактинемије током антипсихотичке терапије последица је централне блокаде допаминских рецептора у хипоталамусу, што доводи до ослобађања пролактина из предњег режња хипофизе. Хиперпролактинемија се најчешће јавља код лечења оланзапином, рисперидоном и амисулпридом.
 [ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
[ 16 ], [ 17 ], [ 18 ], [ 19 ], [ 20 ]
Агранулоцитоза
Још једна озбиљна компликација антипсихотичке терапије. Може се приметити током лечења клозапином и оланзапином. Према Ј. Гедесу и др. (2000), дијагностикована је током прва 3 месеца код 1-2% пацијената који узимају ове лекове. У том смислу, препоручују се недељне анализе крви за пацијенте који узимају ове лекове током првих 18 недеља терапије и месечно праћење након тога. Показано је да када се смањи доза горе поменутих неуролептика, клиничка анализа крви се враћа у нормалу. Истовремено, треба признати да до данас не постоји јасна стратегија за пацијенте који доживљавају горе поменуте нежељене ефекте повезане са метаболичким поремећајима. Најчешће се један атипични антипсихотик замењује другим. Још један обећавајући правац је именовање посебне корективне терапије, посебно употреба бромокриптина за корекцију хиперпролактинемије. Идеална ситуација је она у којој се брига о пацијенту са таквим поремећајима спроводи уз периодично укључивање интерниста, посебно ендокринолога, кардиолога и других специјалиста.
У закључку, треба напоменути да ако се поштују дати алгоритми за прописивање и праћење не само менталног већ и физичког стања пацијената, употреба лекова друге генерације је безбеднија од типичних неуролептика.
Бројни други антипсихотици су тренутно у фази развоја. Лекови следеће генерације ће вероватно имати другачији механизам деловања (на пример, ГАБАергички профил) и моћи ће да утичу на различите манифестације шизофреније, укључујући и саме поремећаје дефицита.
Пажња!
Да бисте поједноставили перцепцију информација, ова упутства за употребу дроге "Неуролептици или антипсихотици" су преведена и представљена у посебном облику на основу званичних упутстава за медицинску употребу лека. Пре употребе прочитајте примедбу која је долазила директно на лек.
Опис обезбеђен у информативне сврхе и није водич за самоделивање. Потреба за овим леком, сврху режима лечења, метода и доза лека одређује само лекар који присуствује. Само-лек је опасан за ваше здравље.

