
Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Како ембрион „загриза“ мајчино ткиво: механика имплантације код људи снимљена у реалном времену по први пут
Последње прегледано: 23.08.2025
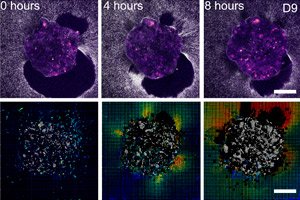 ">
">Научници из Барселоне (IBEC, Dexeus Mujer) и Тел Авива су први пут у реалном времену и у 3Д приказу показали како се људски ембрион причвршћује за „материчну скелу“ и буквално вуче и реструктурира околно ткиво. Да би то урадили, створили су деформабилну ex vivo платформу (колаген/ECM гелови) и применили микроскопију вучне силе директно на живе људске и мишје ембрионе. Кључно откриће: образац сила је специфичан за врсту, а сами ембриони су механосензитивни: реагују на спољашње механичке сигнале реструктурирањем цитоскелета и променом оријентације раста.
Позадина студије
Имплантација је „уско грло“ људске репродукције: управо у овој фази и природна зачећа и покушаји вантелесне оплодње најчешће не успевају. Истовремено, људска имплантација је интерстицијална: ембрион се не „залепи“ једноставно већ је потпуно уграђен у ендометријум – биохемијски и механички сложен процес, али донедавно готово непримећен у живим системима код људи. Стога је механика адхезије и инвазије остала „црна кутија“, а закључци су често доношени на основу индиректних маркера или података са животињских модела.
Класична биологија имплантације се у великој мери ослањала на мишеве, али постоје фундаменталне разлике између врста, од оријентације бластоцисте до дубине имплантације и обрасца ћелијских сила. Код мишева је имплантација „површнија“, са преференцијалним правцима померања ткива; код људи је изразито инвазивна, са мултифокалним силама вуче око ембриона. Ове разлике указују на то да се мишји модел не скалира увек за људе, посебно када је у питању механика. Била су потребна директна посматрања људског ембриона у деформабилном окружењу.
Технолошки пробој је омогућен комбиновањем деформабилних 2Д/3Д матрица (колаген/ECM) и микроскопије трактационе силе са дугорочним снимањем високе фреквенције. Ова „вештачка материца“ је омогућила да се буквално види и измери како ембрион вуче, реструктурира и „буши“ околно ткиво – и како реагује на спољашње механичке сигнале (механосензитивност). Ово отвара пут новим критеријумима за процену потенцијала имплантације и фином подешавању услова трансфера ембриона.
Контекст је примењен: ако су механичка својства окружења и образац ембрионалних сила повезани са успехом имплантације, онда је у вантелесној оплодњи могуће намерно одабрати крутост/састав матрице, узети у обзир временске прозоре трансфера, па чак и користити метрике „силе“ као додатни маркер селекције. Паралелно, такве платформе ће помоћи да се објасни удео раних губитака трудноће, када је биохемија „нормална“, али механика адхезије није. Све ово чини директна 3Д посматрања људске имплантације не само прелепим видеом, већ и новим алатом за репродуктивну медицину.
Зашто је ово важно?
Неуспех имплантације је један од главних узрока неплодности и до 60% спонтаних побачаја. Упркос биохемијском напретку у вантелесној оплодњи, механика овог процеса код људи је остала „црна кутија“. Нови приступ нам омогућава да видимо силе и путање имплантације ембриона и пружа основу за побољшање услова селекције и трансфера ембриона.
Како је то урађено
Истраживачи су саставили „вештачку материцу“ - меко, провидно и деформабилно окружење у којем се матрица слична ткиву видљиво помера под утицајем ембрионалних сила. Затим је уследила континуирана микроскопија и рачунарска анализа померања влакана.
- 2Д и 3Д платформе: у 3Д, ембрион се одмах уграђује у матрицу (фаза причвршћивања се „заобилази“), што омогућава да се види бушење у дебљину ткива.
- Висока „преживљајност и пенетрација“ у 3Д: око 80% успешне инвазије (ограничено близином стакла).
- Мапе вуче и дигитална корелација запремине показују амплитуде и правце померања око ембриона - у суштини „отисак“ силе током времена.
Шта је тачно пронађено (укратко и тачку по тачку)
1) Механизам имплантације специфичан за врсту
- Човек: ембрион је уметнут у матрицу, стварајући вишеструке жаришта вуче и формирајући радијално униформне померања око себе; дубина инвазије је до 200 µм.
- Миш: ембрион се углавном шири по површини са израженим главним правцима померања.
2) Ембрион осећа механику околине
- Спољашње силе → одговор: код људског ембриона - регрутовање миозина и усмерених ћелијских псеудоподија; код миша - ротација осе имплантације/раста према извору спољашње силе (оријентација ПД осе).
- Механосензитивни маркери: код миша, померања у локализацији YAP-а у трофобласту; заједно ово указује на механосензитивно повратно коло.
3) Однос између снаге и успеха имплантације
- Мање померање колагена → лошији напредак имплантације код људских ембриона.
- Интегрини - „спојница“ снаге: блокада RGD пептида/инхибиција Src код мишева смањује дубину/површину имплантације.
Како изгледа имплементација?
- На 2Д и 3Д платформама, око ембриона се формира растући „ореол“ померања влакана; мапа вуче пулсира као да ембрион „скенира“ своју околину.
- На стаклу, људски ембрион формира раван израстак, али у мекој матрици остаје сферичнији и иде дубље - као у живом ткиву.
Шта ово даје пракси (перспективе за вантелесну оплодњу и не само)
Идеја је једноставна: имплантација није само „хемија рецептора“, већ и механика адхезије и вуче. То значи да можемо оптимизовати:
- Тврдоћа материјала и медијума током тестова потенцијала културе/имплантације;
- Нови маркери за селекцију ембриона - засновани на трајекторијама и амплитуди померања у „паметној“ матрици;
- Тренинг/модулација материце (нпр. путем нежних механичких подстицаја) ради побољшања адхезије без агресивних интервенција.
Опрез: ex vivo рад није „унутар материце“. Али сама чињеница да спољашњи механички сигнал мења оријентацију имплантације/организацију оса отвара пут персонализованим условима ембриотрансфера.
Ограничења
- Еx vivo модел не узима у обзир имунолошку, хормонску и васкуларну динамику стварног ендометријума;
- Матригел/колаген дефинишу скуп својстава (крутост, вискоеластичност, састав), тешко их је променити једним параметром;
- Етичка ограничења за студије на људима (период до 14 дана) ограничавају дугорочно посматрање. Међутим, висока сагласност са познатим начинима имплантације in vivo (интерстицијска код људи наспрам површинске код мишева) повећава поверење у модел.
Закључак
Људски ембрион активно „вуче“ и „буши“ свој пут у мајчино ткиво, а механички сигнали из околине могу да реконфигуришу његово понашање. Образац сила и стратегија имплантације су различити код људи и мишева - и то може објаснити зашто модел миша не предвиђа увек успешну имплантацију код људи. Механика је сада пуноправни играч у раној ембриологији и репродуктивној медицини.
Извор: Годо АЛ и др. Сила вуче и механосензитивност посредују у специфичним обрасцима имплантације код људских и мишјих ембриона. Science Advances 11(33): eadr5199 (15. август 2025). DOI: 10.1126/sciadv.adr519
