
Сви иЛиве садржаји су медицински прегледани или проверени како би се осигурала што већа тачност.
Имамо стриктне смјернице за набавку и само линкамо на угледне медијске странице, академске истраживачке институције и, кад год је то могуће, медицински прегледане студије. Имајте на уму да су бројеви у заградама ([1], [2], итд.) Везе које се могу кликнути на ове студије.
Ако сматрате да је било који од наших садржаја нетачан, застарио или на неки други начин упитан, одаберите га и притисните Цтрл + Ентер.
Експерименти показују како ћелије рака избегавају гладовање и смрт од хемотерапије
Последње прегледано: 02.07.2025
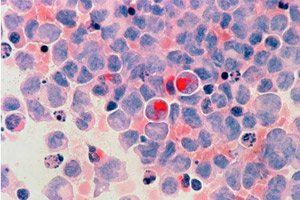
Лабораторијски експерименти са ћелијама рака открили су два кључна механизма који омогућавају туморима да избегну лекове дизајниране да их убију блокирајући њихов метаболизам.
Хемотерапија, иако ефикасна у лечењу рака и продужавању преживљавања пацијената, често губи своју ефикасност због способности ћелија рака да препрограмирају своје метаболичке процесе како би преживеле. Многи лекови у категорији антиметаболита делују тако што ометају процесе неопходне за раст и преживљавање тумора, као што је синтеза пиримидина, молекула који чине основу нуклеотида РНК и ДНК.
Кључни налази студије
Механизам деловања лека и избегавање тумора
- Лекови који се користе у студији (ралтитрексед, PALA, бреквинар) блокирају синтезу пиримидина, што доводи до исцрпљивања њихових резерви у ћелији и, на крају, до апоптозе (програмиране ћелијске смрти).
- Међутим, у окружењу са ниским садржајем глукозе (микроокружење тумора), ћелије рака успоравају коришћење расположивих резерви пиримидина. Ово успоравање спречава хемотерапију да ефикасно делује, јер су исцрпљене резерве пиримидина потребне за покретање ћелијске смрти.
Последице ниског нивоа глукозе
- Низак ниво глукозе омета активацију BAX и BAK протеина, који покрећу апоптозу уништавањем митохондрије ћелије.
- Смањени нивои глукозе такође успоравају конверзију једног облика пиримидина (УТП) у други потребан за ћелијске процесе (УДП-глукоза).
Гени кључни за преживљавање
- Анализа 3.000 гена повезаних са ћелијским метаболизмом открила је да је већина њих укључена у синтезу пиримидина, потврђујући да је овај метаболички пут критичан за преживљавање ћелија рака у условима са ниским садржајем глукозе.
Практични значај
Студија баца светло на механизме којима ћелије рака преживљавају у неповољним условима и отвара перспективе за нове терапијске приступе:
Развој нових комбинација хемотерапије:
Будући лекови могу „преварити“ ћелије рака да се понашају као у нормалном окружењу глукозе, чинећи лечење ефикаснијим.Дијагностика и прогноза:
Способност развоја тестова за одређивање како тумор одређеног пацијента реагује на услове са ниским нивоом глукозе помоћи ће у персонализацији лечења.Истраживање алтернативних путева:
Блокирање додатних метаболичких путева у ћелијама рака ради индуковања апоптозе. Посебно, инхибитори Chk-1 и ATR су обећавајући путеви, иако подношљивост пацијената остаје ограничење.
Следећи кораци
Истраживачи планирају да наставе да проучавају друге метаболичке путеве и механизам којим се апоптоза покреће у условима ниске глукозе како би идентификовали додатне циљеве за хемотерапију. Ово би могло значајно побољшати исходе лечења и проширити могућности за борбу против резистентних облика рака.
Студија је објављена у часопису Nature Metabolism.
